 |
| |
 |
| |
 |
府中メディカルプラザ多摩総合医療センター 成人心臓血管外科 部長 大塚俊哉 |
| |
| 心房細動は、1年間で約50万人が罹患する脳梗塞の最大の原因(30%以上)になるという恐ろしい一面を持ち、さらなる画期的な治療法の進化が望まれている。
孤立性(=弁膜症などの他の心臓病変がない)心房細動に対する治療戦略は、保存的治療(抗不整脈薬、電気ショックなど)に抵抗性の場合に観血的な方法へ進むというのが一般的1)である。この観血的治療の第一選択肢として、多くの場合、内科医によるカテーテルを用いたアブレーションが好まれている。
歴史的には古い従来の心臓外科手術的治療法(メイズ法など)はその“根治性"という利点がありながら“侵襲性=人工心肺や胸骨正中切開"という側面が嫌われ、孤立性心房細動の治療法としては例外的な選択肢の地位に甘んじているのが現状である。しかし、手術手技や手術器械のめざましい進歩により、侵襲性(=患者に対する身体的負担)を大きく軽減する手法が次々と誕生し、心房細動の治療にもその波が押し寄せつつある。
米国のWolfら2)が近年開発した心房細動に対する新しい術式がその低侵襲性と卓越した臨床成績ゆえに脚光を浴びるのを知り、著者らはこの手術法を導入し発展させ本邦で初めての内視鏡下心房細動根治手術を行った。本稿ではこの手術法を解説し、臨床結果について報告する。 |
| |
| 全手術例(20例:男性18名、女性2名、平均年齢58±10。2歳)が孤立性心房細動症例で、病型は発作型が4例、 慢性型が16例(心房細動歴1-4年、平均2。5±6。8年)であった。
術前行った経胸壁心臓超音波検査において平均左房径は43±5。2mm(38-52mm)であった。既往歴は本態性高血圧症2例(10。0%)、糖尿病2例(10。0%)で慢性型の1例にカテーテルアブレーション歴があった。 |
| |
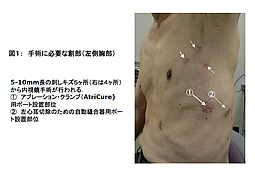 |
| 図1
|
|
|
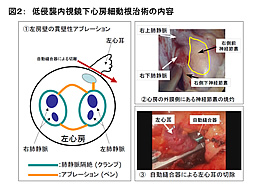 |
| 図2 |
|
| |
 |
|
|
| 図3 |
| 〔麻酔と体位〕
全身麻酔下の両側の腋窩を広く露出するよう両上肢を挙上した仰臥位。
〔手術に必要な皮膚の刺しキズ: 図1〕
約5-10mm長の刺しキズを左側胸壁に5ヶ所、右側に4ヶ所設け、ポートと呼ばれる筒状のものを設置し、これを通して内視鏡や手術器械類を胸腔内に挿入する。
〔心膜切開〕
横隔神経の走行を確認し、心膜を神経の前方1。5-2。0cmで神経に沿って縦切開する。
〔アブレーションおよび左心耳切除: 図2〕
左側は左肺動脈と左上肺静脈の間にあるマーシャル靭帯を切離し、鈍的剥離により左房後方の心膜洞にいたる。右側は下大静脈と右下肺静脈の間および右上肺静脈と右肺動脈の間を鈍的に剥離し心膜洞に至る。
剥離操作ののちこの手術のために開発されたバイポーラ・ラジオ波肺静脈隔絶用クランプ (図3:AtriCure、USA)を使用して肺静脈基部を完全にクランプしペーシングテストにより確認しながら2-3回(1回20秒程度)のアブレーションを行う。
さらに左側はペン型(図3)を用い肺静脈の隔絶線と左心耳との間をアブレーションし、加えて慢性型心房細動症例では左房天井およびいわゆるボックスラインと呼ばれる部位の焼灼を行う。右側ではやはりペン型を用い上大静脈の内側と右房の前面の脂肪織(神経節叢)の焼灼を行う(図2:②)。
左心耳切離は内視鏡手術用自動縫合器(図3: EZ-45、Ethicon、USA)を用いて行う(図2:③ 【参照動画】)。
心膜は両側共に内視鏡用持針器を使用して2針程度で寄せておく。 |
| |
 |
|
|
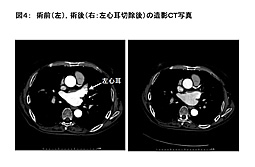
図4 |
死亡、重大合併症、輸血症例はなし。人工心肺または開胸アプローチへの移行もなく平均手術時間は左側が44±11。5分、右側が32±8。8分。平均術後入院期間は5。5±2。5日。平均術後経過観察期間は10。6±7。5ヶ月で6ヶ月以上経過した14例の整脈復帰率は発作型(4例)=100%、 慢性型(10例)=80%であり、薬剤離脱率はワーファリン=78。6%、抗不整脈薬=71。4%であった。また全例において術後造影CTにより左心耳の完全切除を確認(図4)。 |
| |
 |
|
20例の孤立性心房細動症例に対し、バイポーラ・ラジオ波凝固装置および内視鏡手術用自動縫合器を用いた心外膜側からの心房壁アブレーションおよび左心耳切除は完全内視鏡下に低侵襲かつ安全に行え、6ヶ月後の整脈復帰率は発作型心房細動で100%、慢性型で80%と良好な成績であった。
本法の(内科医による)カテーテル法と比べた利点は、まず第1に、Voellerら3)の慢性動物実験で証明されているとおり、 クランプ型のアブレーションによってきわめて短時間(20秒程度)で作成される一様な連続性および貫壁性の保証された心房壁凝固であり、 これによりもっとも重要かつ心房細動治療の主役ともいえる両側肺静脈の電気的隔絶が迅速かつ確実に行える。心嚢内でクランプするので実際は肺静脈基部より1-2cm離れた左心房壁がクランプされアブレーションによる術後肺静脈狭窄の心配もない。次に重要かつカテーテル法では絶対に不可能なセールスポイントは、脳梗塞の原因となる血栓の好発(90%以上)部位である左心耳を切除できるという点である。この手技はである。さらなる利点はアブレーションが心外膜側(心臓の外側)から行われるということにある。心内膜側(心臓の内側)から内→外にエネルギーを伝播させるカテーテル法では食道など心臓周辺臓器に対する致死的な誤焼灼が起こり得るが外→内型の本法ではありえない合併症である。また当然のことながら、カテーテル法では必要不可欠なBrockenbrough手技(=心房中隔の穿破)など心臓内部構造への干渉、悪影響はない。また、心外膜の脂肪組織に内在する交感神経および副交感神経が混在する神経節叢4、5)の迅速かつ安全な焼灼も可能になる。
本法は、心房細動が長期に継続し左心房がすでに6cm超に拡大した症例などの一部の適応外症例を除き、観血的な治療を必要とするすべての心房細動症例に適応できるが、特に、その高い安全性から高齢者など組織が脆弱なケース、または左心耳切除という付加的価値を考慮し、脳梗塞のリスクが高い症例や抗凝固治療が困難な-あるいはワーファリンを飲みたくない-患者に大きな恩恵をもたらしうると思われる。 |
| |
 |
|
孤立性心房細動に対する完全内視鏡下心房細動根治術は安全に行うことができ整脈復帰率などの早期成績は良好であった。本法はカテーテル法に勝る多くの利点を持ちながら心房細動に対する外科的治療の低侵襲化を実現し、心房細動治療の選択肢を画期的に拡げ得る治療法であるといえる。 |
| |
1) 小松聡、相沢義房、新博次、他。心房細動治療(薬物)ガイドライン(2008年改訂版)。Circ J 2008;72(Suppl-IV);1581-1638。
2) Wolf RK。 Minimally invasive surgical treatment of atrial fibrillation。 Semin Thorac Cardiovasc Surg。 2007;19:311-318。
3) Voeller RK、 Zierer A、 Lall SC、 et al。 Efficacy of a novel bipolar radiofrequency ablation device on the beating heart for atrial fibrillation ablation: A long-term porcine study。 J Thorac Cardiovasc Surg。 [In Press]
4) Scherlag BJ、 Nakagawa H、 Jackman WM、 et al。 Electrical stimulation to identify neural elements on the heart: their role in atrial fibrillation。 J Interv Card Electrophysiol。 2005;13(Suppl-1):37-42。
5) Mehall JR、 Kohut RM Jr、 Schneeberger EW、 et al。 Intraoperative epicardial electrophysiologic mapping and isolation of autonomic ganglionic plexi。 Ann Thorac Surg。 2007;83:538-541。 |
| |
|
| |
 |
|